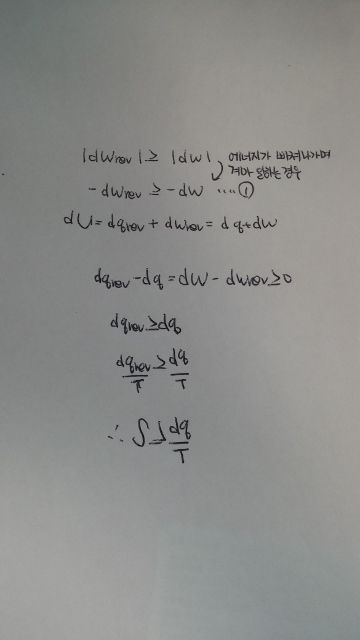열역학 clausius부등식 질문드립니다!
- 글쓴이
- 물려받다
- 등록일
- 2014-07-22 14:08
- 조회
- 9,052회
- 추천
- 0건
- 댓글
- 3건
관련링크
열역학을 공부하던 중에
clausius부등식에서 궁금한 점이 있어서 글을 올립니다.
첨부한 사진에서
가역과정은 비가역과정보다 일을 더 많이 할 수 있으므로
1번식을 유도할 수 있습니다.
그리고 내부에너지는 상태함수이므로 가역과정으로 진행되던 비가역과정으로 진행되던 처음 상태와 나중 상태가 같다면 같으므로 식을 풀어나가면 맨 마지막 식을 도출 할 수 있습니다.
이 식이 clausius부등식 인데 왜 이식을 만족하면 자발적인 반응이라고 하는지 이해가 안됩니다. 단순히 가역과정과 비가역과정을 비교하여 도출한 식에서 자발적인 과정을 어떻게 생각해야하는건지 궁금합니다!!
clausius부등식에서 궁금한 점이 있어서 글을 올립니다.
첨부한 사진에서
가역과정은 비가역과정보다 일을 더 많이 할 수 있으므로
1번식을 유도할 수 있습니다.
그리고 내부에너지는 상태함수이므로 가역과정으로 진행되던 비가역과정으로 진행되던 처음 상태와 나중 상태가 같다면 같으므로 식을 풀어나가면 맨 마지막 식을 도출 할 수 있습니다.
이 식이 clausius부등식 인데 왜 이식을 만족하면 자발적인 반응이라고 하는지 이해가 안됩니다. 단순히 가역과정과 비가역과정을 비교하여 도출한 식에서 자발적인 과정을 어떻게 생각해야하는건지 궁금합니다!!
다른 사람들 의견
-
재료
()
답은 질문에 벌써 써 놓으셨습니다.
가역과정은 비가역과정보다 일을 더 많이 할 수 있으므로,
다른 말로 쓰면 가역과정에서 넣어 준 에너지보다 비가역인 상태에서 항상 에너지를 더 소모하므로 (관찰에 의한 사실)
부등식은 항상 S쪽으로 열리게 되어 있지요 -
물려받다
()
답변 감사합니다!
제가 궁금한 부분은 저 식으로 부터 '자발성이 어떻게 설명되는 가'였습니다. 저 식을 일정 온도와 일정 압력조건에서 정리하게 되면 dG<0이 나오게 되는데 이는 자발성의 척도가 됩니다.
clausius부등식은 단순히 가역과정과 비가역과정을 비교한 식인데 갑자기 저식으로 '왜 자발성이 설명되는가'를 이해 못하겠습니다! -
재료
()
지금 뭔가 잘못 생각하고 있는데
클라우시스는 열역학 2법칙을 만든 사람이 아닙니다.
비가역과정에서 에너지를 언제나 잃는다는 사실은 클라우시스 식을 보고 알게 된 게 아닙니다. 관찰된 사실이죠.
클라우시스는 상기 관찰된 사실 (열역학 2법칙)을 수식으로 나타낸 겁니다.
여러 복잡한 반응계에서 G 만 고려하면 자발성을 알 수 있으므로 유용한거지요.